Kroonilise südamepuudulikkusega patsiendi käsitlus esmatasandil ja suunamine südamepuudulikkuse kabineti õe iseseisvale vastuvõtule
Perearstidel on täita keskne roll kroonilise südamepuudulikkusega patsiendi raviteekonnal. Esmatasandi ülesanne on teha südamepuudulikkuse kahtlusega patsiendil esmane diagnostika, osaleda multidistsiplinaarse meeskonna töös perioodil, mil patsient on spetsialisti jälgimisel, ning tagada palliatiivne ravi (1).

Südamepuudulikkus (SP) on sage kliiniline sündroom, mis esineb valdavalt vanemaealiste populatsioonis ning on vananevas ühiskonnas selges kasvutrendis. Kroonilist südamepuudulikkust esineb Euroopas keskmiselt 1–2%-l elanikkonnast ning üle 70-aastaste inimeste hulgas rohkem kui 10%-l (2). Oluline on kroonilist südamepuudulikkust õigeaegselt diagnoosida ning alustada tõenduspõhist ravi. Ravi ei taga küll tervistumist, kuid mõjutab soodsalt haiguse kulgu, parandades seejuures patsiendi elukvaliteeti, prognoosi ning vähendades hospitaliseerimist.
Sagedasem sümptom on õhupuudus
Enamus patsientidest, kellel on diagnoositud krooniline südamepuudulikkus, saavad diagnoosi perearsti juures. Õhupuudus on sagedasem pöördumise põhjus vanemaealistel ja peamine kroonilise südamepuudulikkuse sümptom. Igal kuuendal üle 65-aastasel koormusdüspnoega patsiendil jääb südamepuudulikkus diagnoosimata (3). Näiteks NYHA (New York Heart Association) klassifikatsiooni II klassi südamepuudulikkusega patsiendil esineb kerge füüsilise aktiivsuse piirang. Rahuolekus on patsient kaebusteta, kuid juba tavaline füüsiline koormus põhjustab väsimust, südamepekslemist ja düspnoed. Diferentsiaaldiagnostiliselt tuleb õhupuudust kaebaval patsiendil välistada krooniline obstruktiivne kopsuhaigus, bronhiaalastma, kopsuarteri trombemboolia, rasvunud patsientidel obstruktiivne uneapnoe ja aneemia. Kopsupatoloogia välistamiseks on soovitatav teha rindkere röntgenuuring ja spirograafia, täiendavalt vereanalüüsidest hemogramm ja d-dimeer aitavad välja lülitada kroonilise aneemia ja tromboosi.
2016. aasta Euroopa Kardioloogide Seltsi ravijuhend
2016. aastal avaldatud Euroopa Kardioloogide Seltsi ägeda ja kroonilise südamepuudulikkuse ravijuhendis on väga hästi kirjutatud lahti SP diagnoosi kriteeriumid ning toodud ära diagnoosimise ja ravi algoritm, mis on hõlpsasti rakendatavad igapäevapraktikas.
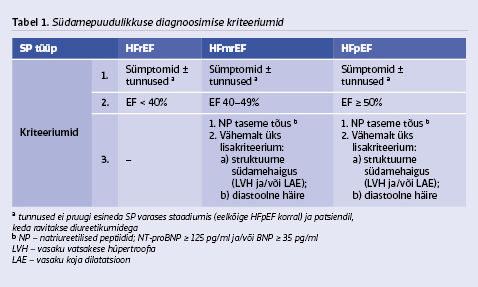
1. SP diagnoosi kriteeriumid
Kroonilise SP diagnoosimiseks peavad olema täidetud kindlad kriteeriumid. Alustades iseloomulikest tüüpilistest sümptomitest, näiteks õhupuudus, koormustaluvuse vähenemine, väsimus ja pahkluude piirkonna turse, ning objektiivsetest tunnustest, näiteks kõrge jugulaarveenide rõhk, paisuräginad kopsudes ja perifeersed tursed. Ehhokardiograafiliselt on vaja dokumenteerida südame struktuurne või funktsionaalne häire ja vastavalt vasaku vatsakese väljutusfraktsioonile klassifitseerida säilinud (HFpEF, EF ≥ 50%) või mõõdukalt vähenenud (HFmrEF, EF 40–49%) või vähenenud väljutusfraktsiooniga (HFrEF, EF < 40%) SP.
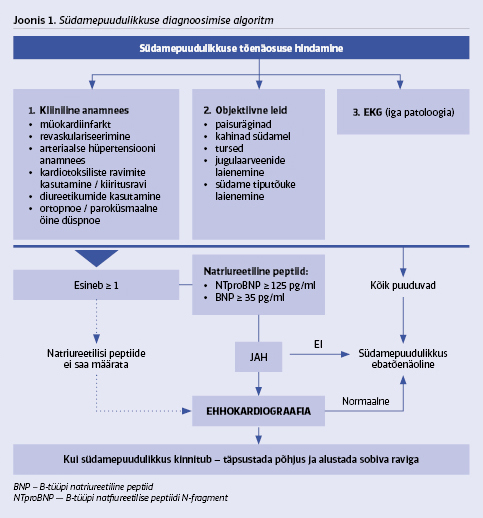
2. SP diagnoosimise algoritm
Südamepuudulikkuse kahtlusel tuleb hinnata diagnoosi tõenäosust, seda, milline on patsiendi kardiaalne anamnees ja objektiivne leid. Vaja on teha elektrokardiogramm (EKG).
- EKG: patoloogiline EKG suurendab SP diagnoosi tõenäosust, kuid on vähese spetsiifilisusega. EKG alusel saab hinnata varem läbipõetud müokardiinfarktile iseloomulikke muutuseid, leida viiteid ravi näidustuseks: näiteks antikoagulatsioon kodade virvendusarütmia, elektrokardiostimulatsioon siinussõlme nõrkuse sündroomi, resünkroniseeriv ravi laia QRS-kompleksi leiu korral. SP on ebatõenäoline, kui EKG on patoloogiata.
- Natriureetilised peptiidid (NP): natriureetiliste peptiidide plasmakontsentratsiooni määramine on laialt levinud ja kergesti tehtav vereanalüüs, mis on esmavalik SP diagnoosimisel. Praegu määratakse Eestis enamikus laboritest B-tüüpi natriureetilise propeptiidi N-fragment (NT-proBNP), mille referentsväärtusest väiksem kontsentratsioon välistab eelnevalt ravimata patsiendil suure tõenäosusega südamepuudulikkuse.
- Ehhokardiograafia: uuring on perearstide tegevusfondist rahastatavate teenuste nimekirjas, seega on võimalik ilma kohe spetsialistile suunamiseta kinnitada või välja lülitada SP diagnoos.
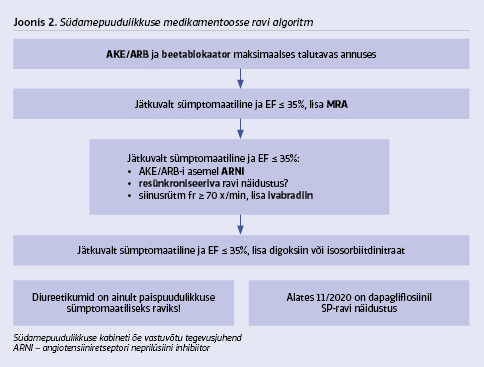
3. HFrEF (EF < 40%) SP medikamentoosse ravi algoritm
Vasaku vatsakese vähenenud väljutusfraktsiooniga SP etioloogia on heterogeenne. Domineeriv foonhaigus on teadaolev krooniline koronaarhaigus (4). Harvem on müokardi kahjustus tingitud toksilistest ainetest (nt alkohol, narkootikumid, tsütostaatikumid) ja viirustest. Kardiomüopaatia võib olla ka geneetiliselt determineeritud.
Euroopa Kardioloogide Seltsi ravijuhend määratleb esmavaliku ravimitena kroonilise SP-ga patsientidel kolm ravimirühma: AKE inhibiitorid (nende talumatusel angiotensiin II konverteeriva ensüümi inhibiitorid ehk ARB-id), beetablokaatorid (BB) ja mineralokortikoidiretseptori antagonistid (MRA) (3).
Vastavalt Euroopa Kardioloogide Seltsi 2016. aasta ravijuhendile on ARNI soovitatud kui asendus AKE inhibiitorile eesmärgiga veelgi vähendada SP hospitaliseerimiste ja surma riski ambulatoorsetel patsientidel, kellel vasaku vatsakese väljutusfraktsioon on vähenenud ja kes on jätkuvalt sümptomaatilised, hoolimata ravist AKE inhibiitori, beetablokaatori ja MRA-ga.
Praegu on Eestis sakubitriili/valsartaani esmase väljakirjutamise õigus kardioloogil ja sisehaiguste arstil kroonilise südamepuudulikkusega täiskasvanud patsientidele, kes vastavad kõigile järgnevatele kriteeriumitele: esineb vasaku vatsakese vähenenud väljutusfraktsioon (LVEF ≤ 35%), patsient kuulub NYHA II–IV funktsionaalklassi, tema ravikoostöö on hea, teda on eelnevalt vähemalt kolm kuud püsivalt ravitud Euroopa ravijuhendi järgi AKE/ARB-i + BB-ga, millele on lisatud MRA, ning tema südamepuudulikkuse sümptomid endiselt püsivad või süvenevad.
Tõenduspõhiste ravimite annuste ülestiitrimine ambulatoorselt eesmärk- või maksimaalselt talutava annuseni on oluline, et parandada patsiendi prognoosi ning vähendada hospitaliseerimist (6). ARNI-raviga paraneb täiendavalt patsiendi elukvaliteet ja funktsionaalne võimekus (7).
SGLT2 inhibiitorid SP raviskeemis
Naatriumi-glükoosi kaastransportija 2 (SGLT2) inhibiitorid on olnud juba Euroopa Kardioloogide Seltsi diabeedi, prediabeedi ja kardiovaskulaarhaiguste 2019. aasta ravijuhendis soovituslikud ravimid 2. tüüpi diabeedi ja kaasuva raske südame-veresoonkonna haiguse korral, kuna avaldavad kardiovaskulaarset suremust vähendavat mõju (8). Eestis on sellest ravimirühmast kasutusel dapagliflosiin ja empagliflosiin. Kui seni on SGLT2 inhibiitorid lubatud suure kardiovaskulaarse riskiga 2. tüüpi diabeetiku raviskeemis, siis 2020. aasta novembrist on dapagliflosiinil Euroopa Ravimiametilt heakskiit täiskasvanute kroonilise sümptomaatilise HFrEF ravis. Kanada Kardioloogide Seltsi 2020. aasta ravijuhendis on dapagliflosiin soovitatud tõenduspõhise ravimina vasaku vatsakese mõõduka kuni raske vähenenud väljutusfraktsiooniga südamepuudulikkusega nii diabeediga kui ilma diabeedita patsientide raviks, parandamaks haigete elukvaliteeti, vähendamaks SP sümptomatoloogiat, hospitaliseerimist ja kardiovaskulaarset surma (9).
Ameerika Kardioloogide Kolleegium (ACC) andis 2021. aasta veebruaris välja uue ravisoovituse, mis rajaneb ekspertide konsensusel ning milles soovitatakse HFrEF-i ravis esmavaliku preparaadina kasutada ARNI-t ja täiendavalt südamepuudulikkuse sümptomite esinemisel lisada SGLT2 inhibiitor (10). 2021. aastal on oodata südamepuudulikkuse ravi optimeerimiseks täiendusi ka Euroopa Kardioloogide Seltsi väljaantavas ravijuhendis.
Edasisuunamine spetsialistile ja südamepuudulikkuse kabineti õe iseseisvale vastuvõtule
Kroonilise südamepuudulikkusega patsiendi käsitlus on multidistsiplinaarne ning ravi ohjamine ja patsiendi jälgimine meeskonnatöö. Pärast diagnoosi püstitamist ja tõenduspõhise ravi alustamist on praegu võimalik suunata patsiente nii suuremate keskuste eriarsti kui ka SP kabineti õe iseseisvale vastuvõtule. Õe roll on koostöös raviarstiga patsiendi nõustamine, SP sümptomite ja objektiivsete tunnuste hindamine, kontrollvereanalüüside tegemine, patsiendi funktsionaalse võimekuse hindamine ja ravimite ülestiitrimine vastavalt raviarsti juhistele.
Valminud on ka Eesti Kardioloogide Seltsi südamepuudulikkuse kabineti õe vastuvõtu tegevusjuhend. SP kabineti õde on oluline lüli patsiendi ja raviarsti vahel, tagamaks järjepidevust kroonilise südamepuudulikkusega patsiendi raviteekonnal.
Kasutatud kirjandus
- H Rutten FH, Gallagher J. What The General Practitioner Needs To Know About Their Chronic Heart Failure Patient. Cardiac Failure Review 2016; 2 (2): 79–84.
- Ponikowski P, Voors AA, Anker SD et al. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2016 jul.14; 37 (27): 2129–2200.
- Van Riet EES, Hoes AW, Limburg A, Landman MAJ, van der Hoeven H, Rutten FH. Prevalence of unrecognized heart failure in older persons with shortness of breath on exertion. Eur J Heart Fail 2014; 16: 772–777.
- Lund LH, Global Public Health Burden of Heart Failure. Card Fail Rev. 2017 Apr; 3 (1): 7–11.
- Atherton JJ. Chronic heart failure: we are fighting the battle, but are we winning the war? Scientifica 2012; 2: ID 279731, 1–16.
- Fiuzat M, Assessment of Limitations to Optimization of Guideline-Directed Medical Therapy in Heart Failure From the GUIDE-IT Trial. JAMA Cardiol. 2020; 5 (7): 757–764.
- McMurray et al. Angiotensin–Neprilysin Inhibition versus Enalapril in Heart Failure. N Engl J Med 2014; 371: 993–1004.
- Consentino, et al. 2019 ESC Guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD: The Task Force for diabetes, pre-diabetes, and cardiovascular diseases of the European Society of Cardiology (ESC) and the European Association for the Study of Diabetes European Heart Journal 2019; 00: 169.
- CCS/CHFS Heart Failure Guidelines: Clinical Trial Update on Functional Mitral Regurgitation, SGLT2 Inhibitors, ARNI in HFpEF, and Tafamidis in Amyloidosis. Canadian Journal of Cardiology Volume 2020; 36: 159–169.
- Maddox TM, Januzzi JL, 2021 Update to the 2017 ACC Expert Consensus Decision Pathway for Optimization of Heart Failure Treatment: Answers to 10 Pivotal Issues About Heart Failure With Reduced Ejection Fraction: A Report of the American College of Cardiology Solution Set Oversight Committee. J Am Coll Cardiol. 2021 Feb; 77 (6): 772–810.
Artikli valmimist toetas SIA Novartis Baltics Eesti filiaal.