Euroopa Hüpertensiooni Ühingu kongressil anti ülevaade kõrge vererõhu diagnoosimise ja ravi uuendustest
31. maist kuni 3. juunini toimus Euroopa Hüpertensiooni Ühingu 33. kongress, kus räägiti muuhulgas uutest vererõhuravimitest, anti ülevaade uuringutest, nutiseadmete olulisusest ning pikemalt peatuti ka patsientide isemõõtmiste ning elustiilimuudatuste juures. Kongressil räägitust tegi ülevaate Põhja-Eesti Regionaalhaigla kardioloog ja Euroopa Hüpertensiooni Ühingu auliige Margus Viigimaa.
Artikkel ilmus septembri Lege Artises. Med24 avaldab ajakirjade artikleid valikuliselt. Lege Artist ja teisi meditsiiniajakirju saab tellida siit.
Mis oli kongressi ja uute juhiste põhiteema?
Alustuseks pean ütlema, et varasemalt on Euroopa Hüpertensiooni Ühing (European Society of Hypertension, ESH) ja Euroopa Kardioloogide Selts (European Society of Cardiology, ESC) hüpertensiooni juhised andnud välja ühiselt, kuid seekord annavad mõlemad ühingud välja omad juhised.
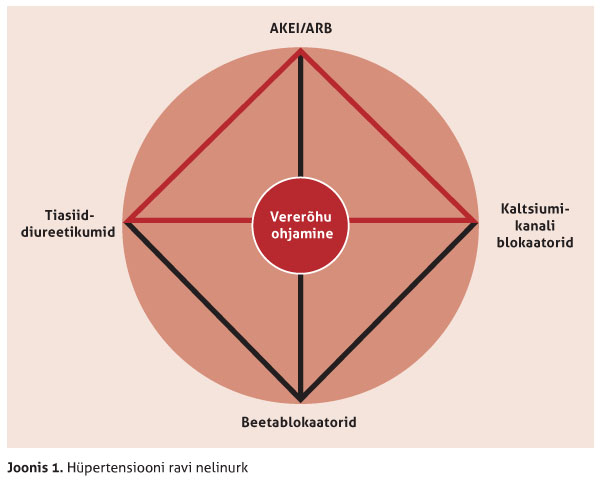
ESH kongressi üks põhiteema oli beetablokaatorite kasutamine ja ravijuhised. Varasemalt on juhistes olnud hüpertensiooni ravi nn kuusnurgana, nüüd aga nelinurgana (vt joonis 1), mille üks komponentidest ongi beetablokaatorid. Selle kohta, kas beetablokaatorid peaksid olema ravi põhikomponent, on olnud tuline diskussioon, praegune juhiste seisukoht on aga selline.
Kehtivates juhistes rõhutatakse, et enamasti vajavad patsiendid kahe ravimi kombineerimist ja paljud neist ka kolme ravimi kombinatsiooni, millest üks on diureetikum. Kõik need komponendid koos annavad ravile tugevama toime, vähema hulga kõrvaltoimeid ning parema ravisoostumuse. Seega saame lähtuda rohkem patsiendipõhiselt ja keskenduda sellele, mida patsient vajab. Enamik patsientidest vajab lisaks statiinravi ja vajadusel selle kombinatsiooni esetimiibiga.
Diagnoosimisest rääkides on uutes juhistes oluliselt suurendatud kodumõõtmiste olulisust, senini on seda alahinnatud. Diagnoosimise kriteeriumid määratakse muidugi jätkuvalt kabinetimõõtmistega ning teine oluline komponent on kindlasti endiselt ambulatoorne monitooring. Kodumõõtmised peaksid muidugi olema tehtud taadeldud aparaadiga ja jälgida tuleb, et patsient mõõdaks oma vererõhku õigesti, sest tegemist on kroonilise haigusega, millega patsient peab elama ja mille raviks ta peab võtma erinevaid ravimeid. Vererõhu mõõtmise õpetus peaks olema perearstil või pereõel patsiendile tehtud ja ka mõõtmisaparaat üle kontrollitud. Eriti just eakatel ja rütmihäiretega patsientidel kipuvad automaatsed aparaadid olema ebatäpsed.
Üks kongressi läbiv teema oli vererõhu langetamine eelkõige elustiili parandamise kaudu ja mittemedikamentoosse ravi osakaalu suurendamine, eriti soolatarbimise vähendamine, füüsilise aktiivsuse suurendamine ja kehakaalu langetamine. Need on teemad, mida peab jälgima tükk aega enne, kui patsiendil hüpertensioon välja areneb. Peame mõjustama mittemedikamentoosset ravi, et patsiendid ei jõuaks ravi vajava kriteeriumini.
Esimest korda on juhistes suurendatud polüpilli osa, ka kvadropilliga on metaanalüüsid nüüdseks tehtud. Tugevalt on sees ka neeruarterite denervatsioon – selle kohta on olemas Euroopa konsensus.
Ameerika Ühendriikides kasutatakse hüpertensiooni diagnoosimisel äralõikepiiri 130/80 mm Hg ja Euroopas 140/90 mm Hg. Kumb on parema tõendusega ja kumba on otstarbekam kasutada?
Selle üle on palju vaieldud, kuid tegelikult on need kõik kokkuleppelised numbrid. Kui vaadata epidemioloogilisi uuringuid, siis kardiovaskulaarsete sündmuste risk, samuti neerupuudulikkuse risk hakkab suurenema süstoolse vererõhuväärtuse 115 mm Hg ja rohkem juures ning diastoolse vererõhuväärtuse 75 mm Hg ja rohkem juures. Kui me selle piiri aga liiga madalaks asetame, võib tekkida probleem eakate ja komorbiidsete patsientidega. Näidud 130/80 mm Hg või 140/90 mm Hg on reaalselt saavutatavad ja patsient mõistab neid. Kui Ameerika Ühendriikides näitude piiri langetati, siis alguses süüdistati neid medikamentoosse ravi propageerimises ning sellega ravimifirmadele kasumi teenimises. Kokkuvõtvalt arvan, et USA ja Euroopa äralõikepiiri erinevustes suurt vahet ei ole.
Korduvalt puudutati hüpertensiooni fenotüüpe ja ravi individualiseerimist. Kas sellel teemal on midagi käegakatsutavat?
Me oleme hästi palju lootnud sellele, et saame abi geneetikast. Hüpertensiooni geneetika on olnud pikalt uurimise all ja viimase 15 aasta jooksul on tehtud selles suunas tohutult edusamme. Meil on Eestis olemas kohort, kuhu kuuluvad nii Tallinna kui ka Tartu patsiendid, ja osaleme selle kohordiga Geenivaramu vahendusel suurtes maailmauuringutes. Kahjuks aga on sinnani veel väga pikk tee, et saaks näiteks geenianalüüsi põhjal leida, kas patsient vajaks raviks mingit teist ravimigruppi või mis ravimigrupp võib patsiendile tekitada rohkem kõrvaletoimeid.
Fenotüüpidest. Üks kindel fenotüüp on näiteks maskeeritud hüpertensioon, mida esineb umbes 10–20%-l juhtudest. Palju räägime ka nn valge kitli sündroomist, mis samuti on üks fenotüüp. Valge kitli sündroomiga peaks me patsienti jälgima, mitte alustama ravi, aga arvestama peab, et 10–15 aasta jooksul areneb sageli välja tõeline hüpertensioon.
Maskeeritud hüpertensiooni korral on patsiendil kabinetis normaalne vererõhk, kuid kui panna ööpäevane monitor peale, siis selgub, et selle keskmine on tegelikult kõrge. Siinkohal tuleks sõeluda neid, kes on ülekaalulised või alkoholi kuritarvitajad, kellel on stress, neerufunktsiooni langus, ja nende puhul peaks mõtlema selle peale, et äkki öösel vererõhk ei lange, mis annabki ööpäevase keskmise normist kõrgema näidu.
Räägiti kardiovaskulaarsest ja renoprotektsioonist n-ö ühe vihmavarju all. Kas lisaks RAAS-blokaatoritele on selles valdkonnas midagi uut oodata? Ameerika Ühendriigid tulid välja oma uue kardiovaskulaarse-renaalse-metaboolse sündroomi kontseptsiooniga, mis on igati loogiline ja need teemad ongi omavahel läbi põimunud. Aga kas see käsitlus on praegu rohkem USA-keskne, sest kongressil käsitleti ainult kombinatsiooni kardiovaskulaarsüsteem-neer?
Tõepoolest tuli see termin USA-s kasutusele varem, kuid sisuliselt ei ole seal vahet – põhimõtteliselt on patsiendigrupp sama ja rohkem on siinkohal tegemist lihtsalt termini erinevusega. Ka Euroopas on hakatud hästi palju rõhutama neerupuudulikkuse või neerukahjustuse osatähtsust ning on saadakse aru, et see on hüpertensiooni tekke üks suurim põhjus.
Kui nimetatud sündroomi defineerida, siis see on olukord, kus patsiendil on ülekaal, prediabeet või diabeet, krooniline neerupuudulikkus ning väga sageli kaasnevad ka kardiovaskulaarsed haigused, näiteks võib tal alguses olla piiripealne südamepuudulikkus või kodade virvendusarütmia, lõpuks arenevad kiiremini välja südame isheemiatõbi, ajuinsult ja perifeersete arterite haigused.
Kui palju räägiti uutest hüpertensiooniravimitest ja kas on tulemas midagi käegakatsutavat?
Meil ei ole uusi hüpertensiooniravimeid olnud 30 aastat, nüüd märtsis 2024 registreeris Ameerika Ühendriikide Toidu- ja Ravimiamet uue ravimi aprotsitentaan, mis on esimene endoteliini retseptori antagonist, mida kasutatakse hüpertooniatõve ravis. See on päris põnev ravim, millega meil Eestis veel kogemust pole. See ravim annab lisavõimalusi ning selle toimemehhanism on erinev neist, mida praegu laialdaselt kasutatakse. Seda saab kasutada ka kombineeritult teiste ravimitega.
Väga perspektiivne ravimiklass on siRNA-tüüpi (väike vaigistav RNA) ravim. Oleme jõudnud hüpertensiooniravis lähedale sellele, et apteekidesse võib peale Ameerika Ühendriikide Toidu- ja Ravimiameti ja Euroopa Ravimiameti registreerimist jõuda ravim nimega zilebesiraan. Osalesime ka selle ravimi uuringutes. Ravim on kaks korda aastas süstitav.
KARDIA-1 uuringus olid mõõduka hüpertensiooniga patsiendid, kelle jaoks oli see ainus ravim. Ööpäevane keskmine ambulatoorne süstoolse vererõhu langus võrreldes platseeboga oli kolme kuu jooksul 14–16 mm Hg. KARDIA-2 uuringus olid väga rasked ja eelnevalt mitmete ravimitega ravitud haiged, kellele manustati zilebesiraani lisaravina. Kolme kuu ööpäevase keskmise ambulatoorse süstoolse vererõhu langus oli zilebesiraan + indapamiid vs. platseebo 12,1 mm Hg, amlodipiin + zilebesiraan vs. platseebo 9,7 mm Hg ja olmesartaani + zilebesiraani rühmas 4,0 mm Hg.
Selline siRNA mehhanismiga ravim on ka kaks korda aastas süstitav kolesteroolialandaja inklisiraan, mida kasutame laialdaselt ka Eestis. Ravim sai selle aasta 1. jaanuarist sajaprotsendilise soodustuse müokardiinfarktijärgsetel ja perekondliku hüperkolesteroleemiaga patsientidel.
Üllatavalt vähe oli juttu diabeediravimitest. Kas SGLT2-inhibiitorid ja muidugi GLP-1 retseptori agonistid eesotsas semaglutiidiga ei tekita hüpertensiooni kontekstis veel furoori?
Kui hakata vaatama, siis diabeedipatsientidel on sageli ka hüpertensioon ja düslipideemia. Selles kontekstis on SGLT2-inhibiitoritest olnud varasemalt väga palju juttu ja need on väga tugevalt hüpertensioonijuhistes sees, samuti diabeedipatsientide südamepuudulikkuse ravijuhistes. Leiti, et SGLT2-inhibiitorid parandavad väga suurel määral diabeedipatsientidel südamepuudulikkuse seisundit. Hiljem teostati ka mittediabeetiliste patsientide uuringuid ning suure edasiminekuna leiti, et esimese preparaadigrupina annavad SGLT2-inhibiitorid positiivse tulemuse ka säilinud vasaku vatsakese väljutusfraktsiooniga patsientidel. Kuni nende ravimiteni olid langenud südamefraktsiooni korral olnud erinevad ravimid efektiivsed, aga säilinud väljutusfraktsiooni korral andsid negatiivse või pluss-miinus-tulemuse.
Seega on SGLT2-inhibiitoritest varasemalt väga palju juttu olnud ja võib öelda, et nüüd on lihtsalt juurde lisandunud GLP-1 retseptori agonistid, sh semaglutiid, mis on väga oluline ravim kaalulangetuse seisukohalt – aga mitte ainult selle jaoks, sest kaalulangetus ise juba parandab hüpertensiooni kulgu ja ravi efektiivsust, samuti erinevaid diabeedipatsientidel esinevaid kardiovaskulaarseid biokeemilisi riskitegureid.
Seega on mõlemad ravimigrupid juhistes eeskätt kaalulangetuse seisukohalt tugevalt sees, sest kui patsiendil on nii diabeet kui ka hüpertensioon, siis peaks ta kasutama ravimeid, mis mõjuvad nii veresuhkrule, vererõhule kui ka kehakaalule.
Kongressil oli juttu ka erinevatest aparaatidest. Patsiendid igatsevad väga usaldusväärset käekella, mis aitaksid vererõhul ja EKG-l pilku peal hoida, ilmselt oleks turgu ka asjalikul nutisõrmusel. Kas on selgunud mingid usaldusväärsemad tootjad ning milline on Euroopas hoiak isemonitoorimise suhtes?
Käekellad ja nutisõrmused on tegelikult väga asjalikud seadmed, kuid omade piirangutega, mida tuleb arvestada. Näiteks näeme sageli, et patsiendid kipuvad saadud tulemusi absolutiseerima.
Positiivne külg on see, et kui visiitidevahelisel perioodil on patsient teinud nutikellaga erinevate parameetrite mõõtmisi, siis on sellest väga-väga palju abi. Me saame selle alusel näiteks hinnata, kuidas toimub patsiendil füüsiliste tegevuste vahel südamelöögisageduse taastumine. Uued nutikellad määravad päris hästi ka vererõhku või on näiteks võimalik salvestada väike EKG-lõik, mille alusel saame vajadusel järeldusi teha. See on hea lahendus olukorras, kus patsient ütleb, et tal oli midagi südamega, aga kiirabi kohale jõudes on episood juba möödunud. Nutikellad aitavad ära tunda ka kodade virvendusarütmiat, mis on kõige sagedasem südamerütmihäire ja algab sageli väga lühiajaliste virvendusepisoodidega.
Nutiseadmed ei pruugi küll olla väga täpsed, kuid algse info me sealt kätte saame. Kindlasti tuleb nende näitajate alusel teha ka põhjalikumad uuringud. Ka võimaldavad need seadmed jälgida unekvaliteeti ja südamelöögisageduse varieerumist, mida patsiendid kipuvad sageli ülehindama.
Tark oleks, kui arst ja patsient lepiksid kokku, mida patsient võiks jälgida, ja ehk võiks ka pereõde patsienti selles osas veidi nõustada. Muidu hakkavad patsiendid saadud andmetest lugema välja midagi, mida seal tegelikult lugeda ei ole, ja nii võib see hakata lõpuks ka ravisoostumust häirima. Ka pole liiga sageli mõtet nutiseadmeid jälgida, sest siis võibki inimene hakata ennast liigselt analüüsima ja ülemäära muretsema.
Üks teema, mida puudutati, oli ka väga eakatel ravimite ära jätmine. Kas selles osas on praktiseerivale arstile mingeid orientiire?
Vahepeal oli probleem, et kui inimene saab näiteks 80- või 85-aastaseks, siis selles vanuses ei ole vererõhu kohta eriti tõenduspõhiseid uuringuid. Tegelikkuses on nüüdseks neid uuringuid tehtud ning leitud, et vanemaealistel toob hüpertensiooniravi sageli kaasa ajuinsuldi riski vähenemise ning seetõttu ei tohiks ravi mingil juhul pooleli jätta. Küsimus on pigem selles, et ühel hetkel võib eaka patsiendi jaoks muutuda ohtlikuks süstoolne vererõhk alla 120, samuti on eakatel patsientidel sageli ortostaatilist hüpotensiooni – patsiendi vererõhuga võib arstikabinetis rahul olla, aga peame siiski alati mõtlema sellele, et tal võib tegelikult olla ortostaatiline hüpotensioon ehk madal vererõhk püsti seistes. Selleks soovitatakse ravijuhistes teha ka mõõtmisi püsti seistes, seda eriti eakatel ja ka diabeetikutel, sest neil on ortostaatilist hüpotensiooni oluliselt sagedamini kui teistel patsiendigruppidel. Mõõtmisi soovitatakse teha ühe minuti ja kolme minuti seismise järel.
Kui vererõhu langus on rohkem kui 20 mm Hg süstoolsel vererõhul ja 10 mm Hg ja rohkem diastoolsel vererõhul, siis saame öelda, et patsiendil on ortostaatiline hüpotensioon. Eakate patsientide puhul on oluline, et me ei tohi vererõhku liiga madalaks viia ja samas ei tohi ka ravi ära jätta. Vahel tekib inimesel ka lisadiagnoose ja terviseprobleeme, siis võime olla raviga tagasihoidlikumad – sageli läheb neeru- ja maksafunktsioon kehvemaks, kehakaal langeb ja lihasmass väheneb ning ravimid võivad hakata toimima tugevamalt ja võime olla ravis tagasihoidlikumad.